- Autor Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:50.
- E modifikuara e fundit 2025-06-01 07:37.
Dallimi kryesor - Metani vs Etani
Metani dhe Etani janë anëtarët më të vegjël të familjes së alkaneve. Formulat molekulare të këtyre dy përbërjeve organike janë përkatësisht CH4 dhe C2H6. Dallimi kryesor midis Metanit dhe Etanit është struktura e tyre kimike; një molekulë etani mund të konsiderohet si dy grupe metil të bashkuar si një dimer i grupeve metil. Dallimet e tjera kimike dhe fizike lindin kryesisht për shkak të këtij ndryshimi strukturor.
Çfarë është metani?
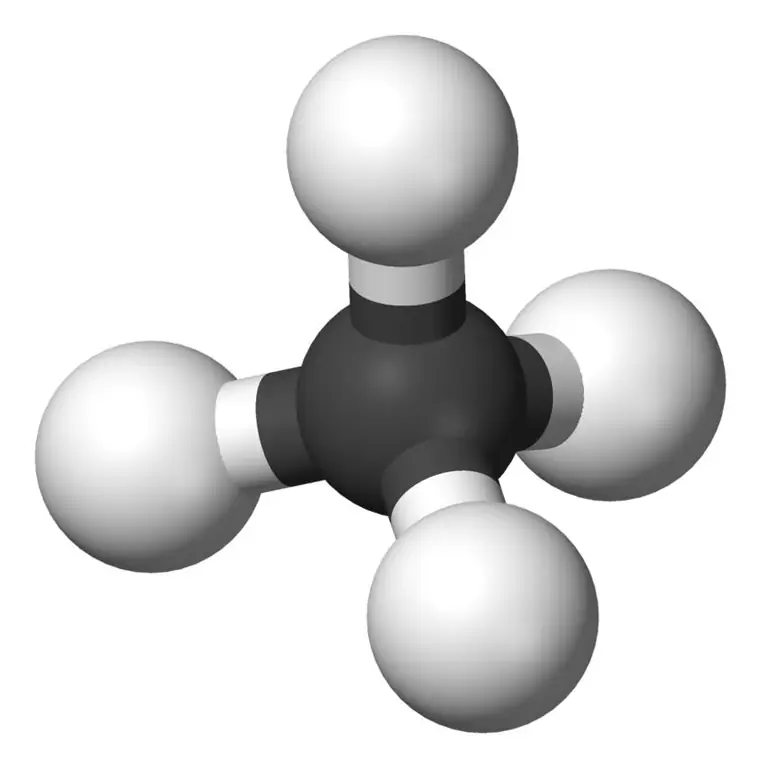
Metani është anëtari më i vogël i familjes së alkaneve me formulën kimike CH4(katër atome hidrogjeni janë të lidhur me një atom karboni). Konsiderohet si përbërësi kryesor i gazit natyror. Metani është një gaz pa ngjyrë, pa erë dhe pa shije; i njohur gjithashtu si karban, gaz kënetor, gaz natyror, tetrahidrid karboni dhe karabit hidrogjeni. Mund të ndizet lehtësisht dhe avulli i tij është më i lehtë se ajri.
Metani gjendet natyrshëm nën tokë dhe nën dyshemenë e detit. Metani atmosferik konsiderohet si gaz serrë. Metani shpërbëhet në CH3- me ujë në atmosferë.
Çfarë është Etani?
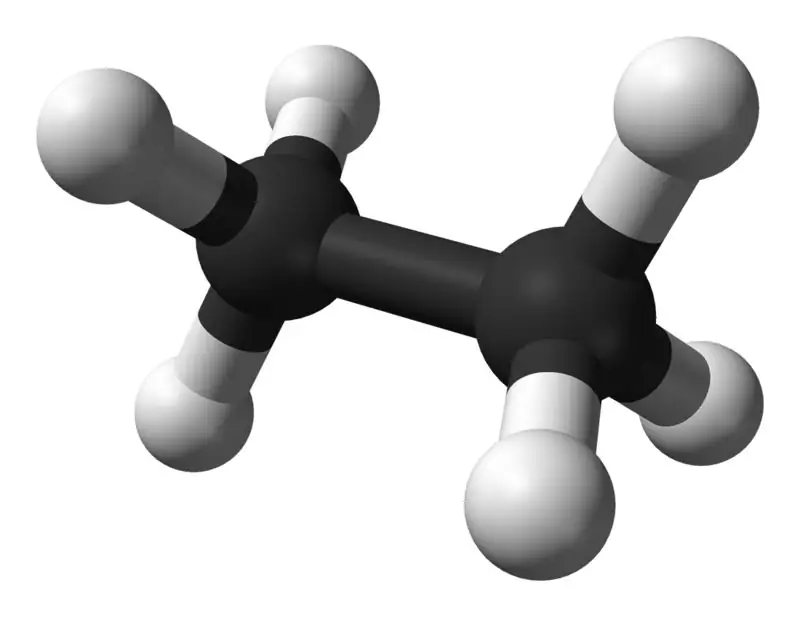
Etani është një përbërje e gaztë pa ngjyrë, pa erë në temperaturë dhe presion standard. Formula e saj molekulare dhe pesha molekulare janë përkatësisht C2H6 dhe 30,07 g·mol−1. Ai është i izoluar nga gazi natyror, si një nënprodukt nga procesi i rafinimit të naftës. Etani është shumë i rëndësishëm në prodhimin e etilenit.
Cili është ndryshimi midis metanit dhe etanit?
Karakteristikat e metanit dhe etanit
Struktura:
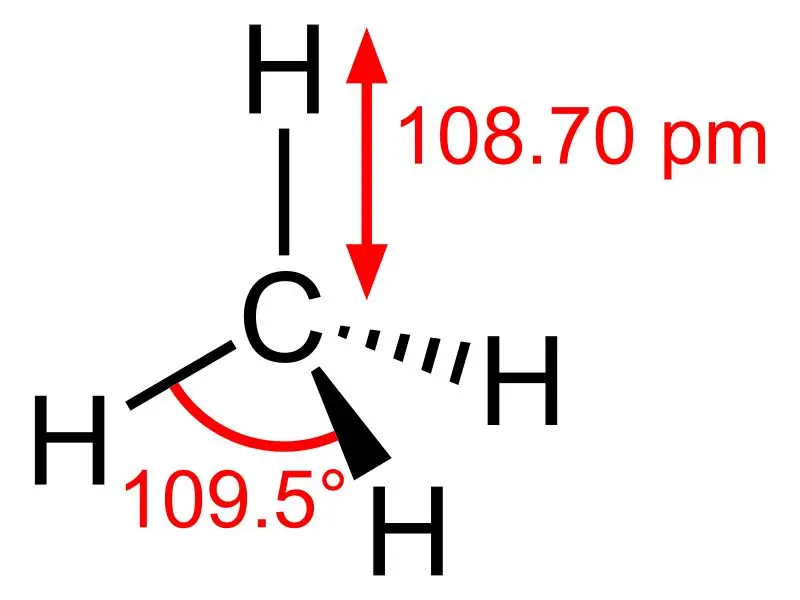
Metan: Formula molekulare e metanit është CH4, dhe është një shembull i një molekule tetraedrale me katër lidhje ekuivalente C-H (lidhje sigma). Këndi i lidhjes ndërmjet atomeve H-C-H është 109,50 dhe të gjitha lidhjet C-H janë ekuivalente dhe është e barabartë me 108,70 pm.
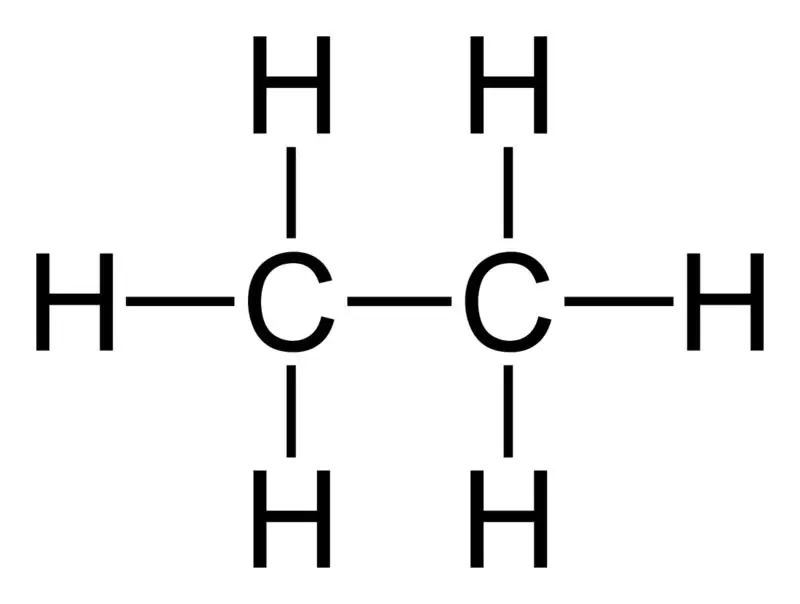
Etani: formula molekulare e etanit është C2H6,dhe është një hidrokarbur i ngopur pasi nuk përmban lidhje të shumta.
Vetitë kimike:
Metan:
Stabiliteti: Metani është një molekulë kimikisht shumë e qëndrueshme që nuk reagon me KMnO4, K2Cr 2O7, H2SO4 ose HNO 3 në kushte normale.
Djegie: Në prani të ajrit ose oksigjenit të tepërt, metani digjet me një flakë të zbehtë blu jo-shndritëse që prodhon dioksid karboni dhe ujë. Është një reaksion shumë ekzotermik; prandaj, përdoret si lëndë djegëse e shkëlqyer. Në prani të ajrit ose oksigjenit të pamjaftueshëm, ai digjet pjesërisht në gaz monoksid karboni (CO).
Reaksionet e zëvendësimit: Metani shfaq reaksione zëvendësimi me halogjene. Në këto reaksione, një ose më shumë atome hidrogjeni zëvendësohen me një numër të barabartë atomesh halogjene dhe quhet "halogjenim". Ai reagon me klorin (Cl) dhe bromin (Br) në prani të dritës së diellit.
Reagimi me avull: Kur një përzierje e metanit dhe avullit kalohet përmes një nikeli të nxehtë (1000 K) të mbështetur në sipërfaqen e aluminit, ai mund të prodhojë hidrogjen.
Piroliza: Kur metani nxehet në rreth 1300 K, ai dekompozohet në karbon të zi dhe hidrogjen.
Etan:
Reaksionet: gazi etan (CH3CH3) reagon me avullin e bromit në prani të dritës për të formuar bromoetan, (CH 3CH2Br) dhe brom hidrogjeni (HBr). Është një reaksion zëvendësimi; një atom hidrogjeni në etan zëvendësohet nga atomi i bromit.
CH3CH3 + Br2 à CH3 CH2Br + HBr
Djegie: Djegia e plotë e etanit prodhon 1559,7 kJ/mol (51,9 kJ/g) nxehtësi, dioksid karboni dhe ujë.
2 C2H6 + 7 O2 → 4 CO 2 + 6 H2O + 3120 kJ
Mund të ndodhë gjithashtu pa një tepricë oksigjeni, duke prodhuar një përzierje të karbonit amorf dhe monoksidit të karbonit.
2 C2H6 + 3 O2 → 4 C + 6 H 2O + energji
2 C2H6 + 5 O2 → 4 CO + 6 H 2O + energji
2 C2H6 + 4 O2 → 2 C + 2 CO + 6 H2O + energji etj.
Përkufizime:
Reaksionet e zëvendësimit: Reaksioni i zëvendësimit është një reaksion kimik që përfshin zhvendosjen e një grupi funksional në një përbërje kimike dhe zëvendësimin e tij nga një grup tjetër funksional.
Përdor:
Metani: Metani përdoret në shumë procese kimike industriale (si lëndë djegëse, gaz natyror, gaz natyror i lëngshëm) dhe transportohet si lëng në frigorifer.
Etani: Etani përdoret si lëndë djegëse për motorët dhe si ftohës për një sistem jashtëzakonisht të ulët të temperaturës. Ai dërgohet në cilindra çeliku si një gaz i lëngshëm nën presionin e tij të avullit.






